水銀化合物の反応
金属水銀とその化合物は、生物に対して非常に毒性があります。 これは、水に非常に溶けやすい化合物に特に当てはまります。 このユニークな元素の組み合わせを実験するときは、細心の注意を払う必要があります(水銀は室温で液体である唯一の金属です)。 化学者の基本的な原則の遵守? 水銀化合物を使って安全にいくつかの実験を行うことができます。
最初の実験では、アルミニウムアマルガム(この金属の液体水銀溶液)を取得します。 水銀(II)溶液硝酸塩(V)水銀(NO3)2 アルミ線(写真1)。 アルミニウム棒(注意深く堆積物を取り除いたもの)を、可溶性水銀塩の溶液とともに試験管に入れます(写真2)。 しばらくすると、ワイヤーの表面から気泡が放出されるのを観察できます(写真3および4)。 溶液からロッドを取り除いた後、粘土がふわふわのコーティングで覆われていることがわかり、さらに、金属水銀のボールも見られます(写真5および6)。
化学 - 水銀を組み合わせる経験
通常の状態では、アルミニウムの表面は酸化アルミニウムのぴったりと合う層でコーティングされています。2O3攻撃的な環境の影響から金属を効果的に隔離します。 ロッドを洗浄して水銀塩の溶液に浸した後、Hgイオンが置換されます2+ よりアクティブなアルミニウム
ロッドの表面に堆積した水銀は、アルミニウムとアマルガムを形成し、酸化物がロッドに付着するのを困難にします。 アルミニウムは非常に活性の高い金属であり(水と反応して水素を放出します。気泡が観察されます)、緻密な酸化物コーティングにより構造材料としての使用が可能です。
XNUMX番目の実験では、NHイオンを検出します。4+ ネスラー試薬を使用(ドイツの化学者ユリウスネスラーは1856年に分析に最初に使用しました)。
ホップと水銀化合物の反応に関する実験
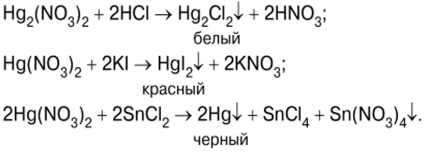
試験はヨウ化水銀(II)HgIの沈殿から始まります。2、ヨウ化カリウムKIと硝酸水銀(II)(V)Hg(NO3)2 (写真7):
HgIのオレンジレッド沈殿物2 (写真8)次に、過剰のヨウ化カリウム溶液で処理して、式Kの可溶性錯化合物を得た。2HgI4 ? ネスラー試薬であるテトラヨージド水銀酸カリウム(II)(写真9):
得られた化合物で、アンモニウムイオンを検出できます。 水酸化ナトリウムNaOHと塩化アンモニウムNHの溶液は引き続き必要です。4Cl(写真10)。 ネスラー試薬に少量のアンモニウム塩溶液を加え、強塩基で培地をアルカリ化した後、試験管の内容物の黄橙色の形成を観察します。 現在の反応は次のように書くことができます:
得られた水銀化合物は複雑な構造を持っています:
高感度のネスラーテストは、水中の微量のアンモニウム塩やアンモニア(水道水など)を検出するために使用されます。

